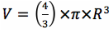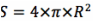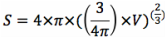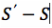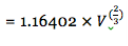I- Les caractéristiques d'une bulle de savon
Qu’est-ce-qu’une bulle ?
C’est une sphère d’eau savonneuse remplie d’air.
C’est une sphère d’eau savonneuse remplie d’air.
A- La molécule d’eau
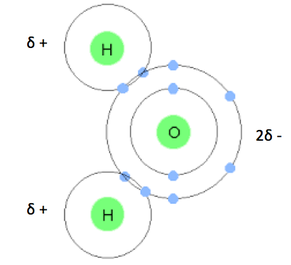
L’eau est la base de la solution à bulles. Cette molécule est constituée de 2 atomes d’hydrogène liés par des liaisons covalentes à un atome d’oxygène.
L’atome d’oxygène possède six électrons au total et cherche deux électrons pour compléter sa couche externe. Chaque atome d’hydrogène possède un électron sur sa couche externe et a besoin d’un seul électron pour devenir stable. Chacun met en commun un électron avec l’atome d’oxygène pour former un doublet.
A cause de cette structure, tous les électrons sont réunis autour du noyau de l’atome d’oxygène, ce qui se traduit par un excès de charges négatives au niveau de celui-ci. Réciproquement, les atomes d’hydrogènes ont un déficit d’électrons et donc sont chargés positivement.
La molécule d’eau est donc polaire. Elle se comporte comme un dipôle : c’est à dire qu’elle a deux charges égales et de signes contraires à une distance fixe l’une de l’autre.
L’eau est la base de la solution à bulles. Cette molécule est constituée de 2 atomes d’hydrogène liés par des liaisons covalentes à un atome d’oxygène.
L’atome d’oxygène possède six électrons au total et cherche deux électrons pour compléter sa couche externe. Chaque atome d’hydrogène possède un électron sur sa couche externe et a besoin d’un seul électron pour devenir stable. Chacun met en commun un électron avec l’atome d’oxygène pour former un doublet.
A cause de cette structure, tous les électrons sont réunis autour du noyau de l’atome d’oxygène, ce qui se traduit par un excès de charges négatives au niveau de celui-ci. Réciproquement, les atomes d’hydrogènes ont un déficit d’électrons et donc sont chargés positivement.
La molécule d’eau est donc polaire. Elle se comporte comme un dipôle : c’est à dire qu’elle a deux charges égales et de signes contraires à une distance fixe l’une de l’autre.
Dans un verre d’eau, les molécules au centre exercent des forces d’attraction sur les molécules voisines: la partie positive de la molécule attire la partie négative des molécules voisines, et vice versa. Ces forces se compensent car les molécules sont entourées de tous les cotés d’autres molécules d’eau et forment un réseau:

B- La Tension superficielle et la pression
Qu’est-ce qui rend la solution à bulle assez “élastique” pour produire une bulle de savon? C’est la tension superficielle. Cette force existe à toute interface entre un liquide et un autre milieu. Dans une masse de liquide, les molécules s’attirent entre-elles. Ces forces se compensent car elles sont entourées de tous les côtés par d’autres molécules. Mais à l’interface avec le deuxième milieu (par exemple l’air) les molécules ne sont attirées que par leurs voisines latérales ou inférieures, créant ainsi un déséquilibre de force. Pour rétablir une structure stable, les molécules à l’interface créent de très fortes liaisons entre elles, et la surface agit comme un film élastique qui peut se déformer. Cette force qui lie les molécules à la surface s’appelle la tension de surface, ou tension superficielle.
Qu’est-ce qui rend la solution à bulle assez “élastique” pour produire une bulle de savon? C’est la tension superficielle. Cette force existe à toute interface entre un liquide et un autre milieu. Dans une masse de liquide, les molécules s’attirent entre-elles. Ces forces se compensent car elles sont entourées de tous les côtés par d’autres molécules. Mais à l’interface avec le deuxième milieu (par exemple l’air) les molécules ne sont attirées que par leurs voisines latérales ou inférieures, créant ainsi un déséquilibre de force. Pour rétablir une structure stable, les molécules à l’interface créent de très fortes liaisons entre elles, et la surface agit comme un film élastique qui peut se déformer. Cette force qui lie les molécules à la surface s’appelle la tension de surface, ou tension superficielle.

Dans l’eau, en raison de la polarité des molécules, il y a de fortes liaisons électrostatiques. Pour avoir une structure stable, la force liant les molécules de surface doit elle aussi être importante. L’eau a donc une grande tension superficielle.
Quand l’on souffle une bulle, c’est la tension superficielle importante de l’eau qui lui permet de se créer et garder sa forme. En effet elle intervient à l’interface entre l’air à l’extérieur de la bulle et l’eau savonneuse, et à l’interface entre l’air à l’intérieur de la bulle et l’eau savonneuse.
Pourtant quand l’on essaye de souffler une bulle dans de l’eau pure, on n’obtient jamais une bulle. Nous pourrions donc penser que la tension superficielle de l’eau pure n’est pas assez importante pour qu’une bulle se forme, et que le savon augmente donc cette force. Ceci est faux! Au contraire, le savon diminue la tension superficielle. Dans la partie II nous expliquerons le rôle du savon.
Dans une bulle de savon, les pressions à l’intérieur et à l’extérieur se compensent presque.
La tension superficielle est étroitement liée à la pression de l’air à l’intérieur et à l’extérieur de la bulle par cette formule :
Où
P1 est la pression atmosphérique en pascals
P2 est la pression de l’air dans la bulle en pascals
λ est la tension superficielle du liquide en newtons par mètre.
R est le rayon de la bulle en mètres.
Quand l’on souffle une bulle, c’est la tension superficielle importante de l’eau qui lui permet de se créer et garder sa forme. En effet elle intervient à l’interface entre l’air à l’extérieur de la bulle et l’eau savonneuse, et à l’interface entre l’air à l’intérieur de la bulle et l’eau savonneuse.
Pourtant quand l’on essaye de souffler une bulle dans de l’eau pure, on n’obtient jamais une bulle. Nous pourrions donc penser que la tension superficielle de l’eau pure n’est pas assez importante pour qu’une bulle se forme, et que le savon augmente donc cette force. Ceci est faux! Au contraire, le savon diminue la tension superficielle. Dans la partie II nous expliquerons le rôle du savon.
Dans une bulle de savon, les pressions à l’intérieur et à l’extérieur se compensent presque.
La tension superficielle est étroitement liée à la pression de l’air à l’intérieur et à l’extérieur de la bulle par cette formule :
Où
P1 est la pression atmosphérique en pascals
P2 est la pression de l’air dans la bulle en pascals
λ est la tension superficielle du liquide en newtons par mètre.
R est le rayon de la bulle en mètres.
C- La forme d’une bulle
On remarque que même si on souffle une bulle à travers un contour carré, triangulaire ou d’autre forme, la bulle sort toujours sphérique. Ceci est dû encore une fois à la tension superficielle, qui fait que le liquide essaye naturellement de diminuer sa surface de contact avec un autre milieu. Pour un volume donné, l’aire doit être minimale.
Pourquoi une sphère ? C’est parce que la sphère est la forme optimale pour répondre à ce problème.
Comparaison d’une sphère et d’un cube :
On cherche à comparer la surface d’une sphère et d’un cube de même volume V.
On remarque que même si on souffle une bulle à travers un contour carré, triangulaire ou d’autre forme, la bulle sort toujours sphérique. Ceci est dû encore une fois à la tension superficielle, qui fait que le liquide essaye naturellement de diminuer sa surface de contact avec un autre milieu. Pour un volume donné, l’aire doit être minimale.
Pourquoi une sphère ? C’est parce que la sphère est la forme optimale pour répondre à ce problème.
Comparaison d’une sphère et d’un cube :
On cherche à comparer la surface d’une sphère et d’un cube de même volume V.
On trouve R par rapport à V
On remplace R dans l’équation de la surface d’une sphère
On trouve C par rapport à V
On remplace dans l’équation de la surface d’un cube
Preuve que la surface d’un cube est supérieure a celle d’une sphère quelque soit V
Remarque : V est positif donc ce produit est forcement positif
Aire du Cube – Aire de la Sphère> 0
Aire de la Sphère <Aire du Cube
Donc la sphère est la forme optimale.
Aire du Cube – Aire de la Sphère> 0
Aire de la Sphère <Aire du Cube
Donc la sphère est la forme optimale.