II- Pourquoi les bulles de savon éclatent-elles?

A- L’évaporation
La raison majeure pour laquelle les bulles de savon éclatent est l’évaporation.
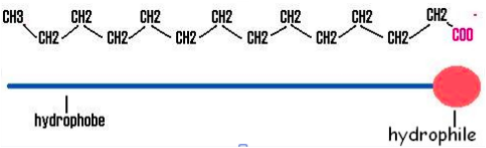
Explorons en premier la structure d’une bulle de savon: la solution de base (eau + liquide vaisselle) est composée de molécules H2O (eau) ainsi que de molécules de savon. Cette dernière est une longue chaîne de carbones et d’hydrogènes.
La « tête » de cette chaîne est constituée d’un groupe carboxylate (COO):
Comme l’eau, ce groupe est polaire, et donc il se lie très bien avec celle-ci. On dit de lui qu’il est hydrophile (qui « aime » l’eau).
Au contraire, la chaîne de la molécule de savon est apolaire, et donc est hydrophobe (qui « n’aime pas » l’eau). Par contre, elle est lipophile car elle est attirée par les matières grasses.
La raison majeure pour laquelle les bulles de savon éclatent est l’évaporation.
Explorons en premier la structure d’une bulle de savon: la solution de base (eau + liquide vaisselle) est composée de molécules H2O (eau) ainsi que de molécules de savon. Cette dernière est une longue chaîne de carbones et d’hydrogènes.
La « tête » de cette chaîne est constituée d’un groupe carboxylate (COO):
Comme l’eau, ce groupe est polaire, et donc il se lie très bien avec celle-ci. On dit de lui qu’il est hydrophile (qui « aime » l’eau).
Au contraire, la chaîne de la molécule de savon est apolaire, et donc est hydrophobe (qui « n’aime pas » l’eau). Par contre, elle est lipophile car elle est attirée par les matières grasses.
Remarque : on peut dire de ces molécules qu’elles sont amphiphiles, car elles présentent une extrémité polaire hydrophile et l’autre est hydrophobe.
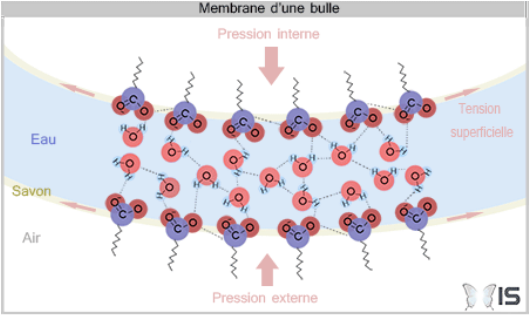
Les molécules hydrophobes qui ne veulent pas être présentes dans la partie aqueuse de la bulle se faufilent entre les molécules d’eau de surface afin d’être positionnées hors de l’eau.
On qualifie ces molécules de tensioactives car elles modifient la tension superficielle en séparant les molécules d’eau l’une de l’autre. La tension superficielle décroit lorsque la distance entre les molécules d’eau augmente ; c’est ce qui se passe lorsque l’on rajoute du savon à de l’eau. Cette réduction est en faite bénéfique car une tension superficielle trop élevée (comme celle de l’eau) déchire la membrane de la bulle. En rajoutant le savon, on obtient une solution avec une tension superficielle optimale.
Les molécules hydrophobes constituent un film de 300nm d’épaisseur à la surface extérieure et intérieure de la bulle, et protègent celle-ci plus ou moins de l’évaporation.
En effet, lorsque l’eau s’évapore, le savon ne peut pas constituer à lui tout seul la bulle. C’est alors que toute sa structure va s’écrouler !
Les molécules hydrophobes qui ne veulent pas être présentes dans la partie aqueuse de la bulle se faufilent entre les molécules d’eau de surface afin d’être positionnées hors de l’eau.
On qualifie ces molécules de tensioactives car elles modifient la tension superficielle en séparant les molécules d’eau l’une de l’autre. La tension superficielle décroit lorsque la distance entre les molécules d’eau augmente ; c’est ce qui se passe lorsque l’on rajoute du savon à de l’eau. Cette réduction est en faite bénéfique car une tension superficielle trop élevée (comme celle de l’eau) déchire la membrane de la bulle. En rajoutant le savon, on obtient une solution avec une tension superficielle optimale.
Les molécules hydrophobes constituent un film de 300nm d’épaisseur à la surface extérieure et intérieure de la bulle, et protègent celle-ci plus ou moins de l’évaporation.
En effet, lorsque l’eau s’évapore, le savon ne peut pas constituer à lui tout seul la bulle. C’est alors que toute sa structure va s’écrouler !
B- Lorsque les bulles rentrent en contact avec une surface
Comme nous l’avons vu plus tôt, un équilibre se forme entre la pression intérieure et extérieure de la bulle (c.f formule).
Cet équilibre est donc très fragile et peut être rompu par une force, si elle est assez grande. Si un trou est créé dans la bulle alors la structure moléculaire fragile s’écroule. Un contact avec notre doigà ou un objet quelconque peut faire éclater la bulle.
Par contre, un objet assez fin et mouillé (une aiguille trempée dans l’eau par exemple) n’a pas une force assez grande pour perturber la structure moléculaire, et les molécules d’ H2O de la bulle se lient avec celles sur l’aiguille.
Comment attraper une bulle dans sa main sans qu’elle éclate ?
Trempez votre main à l’intérieur de la solution à partir de laquelle votre bulle est constituée, et essayez donc ! Les molécules de la bulle de savon se rattachent à celles sur votre main, et la bulle n’éclate pas.
Comme nous l’avons vu plus tôt, un équilibre se forme entre la pression intérieure et extérieure de la bulle (c.f formule).
Cet équilibre est donc très fragile et peut être rompu par une force, si elle est assez grande. Si un trou est créé dans la bulle alors la structure moléculaire fragile s’écroule. Un contact avec notre doigà ou un objet quelconque peut faire éclater la bulle.
Par contre, un objet assez fin et mouillé (une aiguille trempée dans l’eau par exemple) n’a pas une force assez grande pour perturber la structure moléculaire, et les molécules d’ H2O de la bulle se lient avec celles sur l’aiguille.
Comment attraper une bulle dans sa main sans qu’elle éclate ?
Trempez votre main à l’intérieur de la solution à partir de laquelle votre bulle est constituée, et essayez donc ! Les molécules de la bulle de savon se rattachent à celles sur votre main, et la bulle n’éclate pas.
C- Pression et gravité
La bulle, qui est donc composée d’une structure qui lui confère une forme et une élasticité extraordinaire, doit néanmoins se plier aux lois de la gravité.
Nous avons vu que les molécules de savon et d’eau se lient entre elles pour former un film de savon élastique autour de l’air que l’on y souffle. Elles forment une sphère avec un peu d’aide de l’attraction gravitationnelle.
Une fois la bulle formée, la gravité ne va plus lui venir en aide. Le liquide est attiré vers le point le plus bas et commence à couler. Par conséquent, le film d’eau savonneuse devient de plus en plus fin au sommet de la bulle.
Nous l’avons dit, la pression intérieure exerce une force constante sur la surface intérieure de la bulle. Le film est plus fragile au sommet de la bulle, et donc résiste mal à la force qu’exerce la pression intérieure sur elle. La structure de la bulle s’effondre et celle-ci éclate.
La bulle, qui est donc composée d’une structure qui lui confère une forme et une élasticité extraordinaire, doit néanmoins se plier aux lois de la gravité.
Nous avons vu que les molécules de savon et d’eau se lient entre elles pour former un film de savon élastique autour de l’air que l’on y souffle. Elles forment une sphère avec un peu d’aide de l’attraction gravitationnelle.
Une fois la bulle formée, la gravité ne va plus lui venir en aide. Le liquide est attiré vers le point le plus bas et commence à couler. Par conséquent, le film d’eau savonneuse devient de plus en plus fin au sommet de la bulle.
Nous l’avons dit, la pression intérieure exerce une force constante sur la surface intérieure de la bulle. Le film est plus fragile au sommet de la bulle, et donc résiste mal à la force qu’exerce la pression intérieure sur elle. La structure de la bulle s’effondre et celle-ci éclate.